 ����
����
�������в�����Ŀǰ���ϱ���ϵ�������߲������ٴ���ʵ���о�����Ϊ�����������йء�
1.�Ŵ����� 5%�IJ����м��巢��ʷ��������������ͬ������DR2��DR3���á�ĸŮ�Ȼ������Ļ�����ࡣ���������Ŵ�ѧ�о�֤���������������DR2��DR3��ء���C
4aȱ��ʱSLE���������ߡ�Tϸ������ͬSLE���������й�����TNF-����ˮƽ������
�Ǵ����������Ŵ�������
2.�������� ���������������������·�������ʹ�����
(1)������Ⱦ��������ʵ��ʾ����������������(C��RNA����)��Ⱦ�йء�NZB/NEW F1С����֯�з����C��RNA������������С��������в鵽��C�Ͳ������塣�����������δ֤ʵ���κβ�ԭ����ֱ�ӹ�ϵ����ԭ�����ֻ��һ�ֶ��¡Bϸ���̼����ض��ٷ��˱�����
(2)�չ⼰�����ߣ�25%��35%��SLE���˶��չ���������ѧ����Ϊ�������չ��е��������йء������ߵ�����ʹƤ����DNAת��Ϊ������श��������������ԭ�ԣ���ʹ����ϸ����������1����ǿ�����߷�Ӧ��
(3)�Լ��أ���������Ů��Զ������Ϊ�ߣ����ڶ�ͯ�������˴��ֲ�����ԣ���ʾ���������ڴ��Լ���ˮƽ��SLE�ķ�������Ҫ���á�����ʱSLE����ı仯�����Լ���ˮƽ�йء������3���²�����أ����и�Ѫ�дƼ���ˮƽ�����йء��˺�������ͪˮƽѸ�����ߣ���ͪ��ƶ����ı�ֵ��Ӧ���ߣ��Ӷ�ʹ��������ȶ��������м���ˮƽ���ͣ���������ٶȼ��ء��������֣�SLE����Ѫ����������ֵ���ߣ������Լ��صļ̷��Ա仯��������д���һ���о���
(4)ҩ���Щҩ���ǰ뿹ԭ��һ�������Ѵ��ڳ���״̬��SLE�������շ�����Ӧ����շ�SLE֢״������ҩ�������У���ù�ء���ù�ء�ͷ�߾��ء��ǰ��ࡢ��̩�ɡ����Ƽ��ȣ�ͨ��ͣҩ������ֹ���鷢չ����һ��������
�Ǵ����ۺ�����ҩ�������ມ���³�����ȱ�ມ�����Ӣ�ơ������µȡ�����ҩ�ﳤ�ںͽϴ���Ӧ��ʱ���߿ɳ���SLE���ٴ�֢״������ѧ�ı䡣����
ҩ�����Ǵ����ۺ�����ͣҩ��֢״���������˻��������֢״���ˡ�ҩ������
�Ǵ����ۺ������ط���
����Ǵ�������Ϊ�����ٴ������ᣬ�ۼ�����Ƥ������ϵͳ�٣��ڷ�������ϴ۲��̽϶̺����Ѫ�в��岻���٣���Ѫ�嵥��DNA�������ԡ�
(5)������Ʒ��Ѫ��Ʒ��ͨ���������ٴ�ʵ��֤ʵ��������Ʒ������ס����硢ת�����ӡ������ء����ߺ��Ǻ���ȶ����ٴ���SLE������˵�Ǽ��Է��������м������ӣ�һ���������鼱�Է�������ʹͣҩҲ������ֹ�䷢չ���ٴ���SLE������Ѫ(����Ѫ����Ѫ���γɷ֡�����)����ɲ�����ת�IJ���������������ɴ�˵��������Ʒ����Ѫ��ΪSLE���շ����ػ�����ء�
(6)ʳƷ����������ٴ����Ͼ�֤ʵ���ճ���ʳ�ɷֶ�SLE�ķ����в��ɺ��ӵ����á����ҹ��շ�SLE������ʳƷ�У������Ϊ������(�����а��㡢̨���㼰���㣬��ˮ��Ϊ���㡢����)�����̺���Ʒ(������ɡ�����)�����⺬����֬�ص�ʳ����۲ˡ������ȣ������������ʳ���Ģ������Ѭʳ��ȣ���L-���������ʳ�����ޣ�����ӡ����������࣬Ҳ�뱾�ۺ����йء���Щ�����ٴ����������������ӣ����صظ����˻�Ӱ���˲��̵�ת�顣
(7)����������״̬�����ڴ��ڽ�������״̬��������ѹ��״̬�ߣ����Ѵ��ھ�ֹ״̬��SLE�ߣ�һ���ܵ����ؾ���̼������������������ƣ��������շ����鼱�Է�������������ЧӦ��ͨ����-����-�ڷ����������²����á����������SLE��Ů�Զ������ΪŮ�Ե��������ڷ��ڵ������ý�����������ؼ����õĻ��Ǵ��Լ��ضԸ�����ĵ������ý����Լ�������
3.���߷�Ӧ�쳣 һ������ LE �Ŵ����ʵ��ˣ���������������������£�ʹ����������ȶ��������ң�����ΪB�ܰ�ϸ���߶Ȼ�������������������֯������ϸ���˼����ֺ˳ɷ֡�ϸ��Ĥ��ϸ���ʡ�������֯�ɷֵ��������壬�������Կ��˿���Ϊ��Ҫ������Bϸ�����ܿ�����ԭ�������¼����棺�������� Tϸ��ɥʧ�������������ϣ����书���ཱུ�ͣ�ʹ�䲻����Ч�ص���Bϸ�����Ӷ�ʹ�������������γɶ��²�����������Ϊ�����ڸ�����Tϸ�����ܹ�ǿ���������ߵ����ϰ������������������塣����������������ǵ���ϸ�������ϸ���Ļ������ȣ�ͨ������ij�����ӣ��̼�������Tϸ������ֱ�Ӵ̼�Bϸ���������������ߡ����������Ǵ����з���������Bϸ���Ĺ��Ȼ�Ծ����û���ֵ���Tϸ����ȱ�ݣ�����������������B�ܰ�ϸ����������Tϸ���Ŀ��Ƶ��ڣ�����T�ܰ�ϸ�����ڹ�������ʱ�����ܲ����������塣
SLE������ϸ�����ӷ����쳣��IL-1�ɵ���-����ϸ���ϳɣ�����ʹSLE��Bϸ����ֳ���鵼Bϸ������IgG���γ����߸����������֯���ˡ�IL-1���յ�IL-6��IL-8��TNF-�����������Ӳ�������
�Ǵ����������йء�Լ50%����Ѫ����IL-2ˮƽ���ߣ��������л����и�ˮƽ��IL-2R���һ�ڽϻ����ڸߡ�IL-2��Ҫ��CD
4 Tϸ����������SLE����IL-6ˮƽ���ߣ���������ϵͳ�����йء���SLE��ڣ�IL-10ˮƽ���ߣ�IL-10��Bϸ���쳣�������Ҫ���á�
SLE����ѪҺ�г��ֵ����������������¼��ࣺһ��Ϊ���DNA���˵���ϸ���˳ɷֵĿ��壬ͳ��Ϊ���˿��壬����������������������������ߣ�����֪��30���֡�����Щ�����У��еĶ�ij�ּ��������Ըߣ��翹ds-DNA�Ϳ�Sm������SLE�������Կ��塣��νLE���Ӽ���DNA���壬����Ѫ����DNA�γ����߸����������ȫ��������СѪ�ܡ��ڲ������������СѪ���ף�������������ס��ؽ��ס�����Ĥ�ף��Ρ��Ρ�Ƥ�������䡣���˿��������ڰ�ϸ����ϸ���ˣ����߿ɱ�����ϸ�������ɣ���������ϸ����LEϸ����
��һ��Ϊ���Ѫϸ�����������壬�翹��ϸ�����塢����ϸ�����塢��ѪС�忹��Ϳ��ܰ�ϸ�����壬������
��Ѫ��ƶѪ��
������ϸ������֢��
ѪС�������������ܰ�ϸ�����ٵȡ����⣬�������ʪ���ӡ��������忹�塢�����忹�塢����Ѫ���ӿ��弰������֬����ȡ�
 ��������
��������
�������ƣ�SLE����ȫ�������쳣���¶���������Ϊ�����ļ�������������Ϊ����������������߸����������������������߸�����������ڵ�ȱ�ݵ�����֯�����ˡ�
1.Ҫ����SLE�ķ������ƶ������Ȼش������ٴ����� ��SLE���κ������о��з�����ijЩ������������������������ʾ�������Ŵ���������SLE�ڷ����������˺��������и�Ϊ���������ڰ�������ټ������⣬�������ٴ����ֺͲ����ڲ�ͬ����Ļ���Ҳ������ͬ�������������˺Ͷ����˵�SLE���߲���ϰ����ء�Ȼ������Ȥ���ǣ�����������˺��з����ز��ġ�����ʾ�����ĸı��ʹSLE�ķ������ٴ����ַ����仯����ijЩ�������أ������Ե������������䣬���շ������SLE�����⣬����ijЩҩ��������຺������µȣ�Ҳ���յ�����SLE��֢״����SLE��Ҫ�����������举Ů�������Ժ��������ټ������⣬����Ļ�Ի����������Լ���ˮƽ�����ڱ仯����������������Ͳ��顣�ڷ�����ҩҲ���շ������SLE��
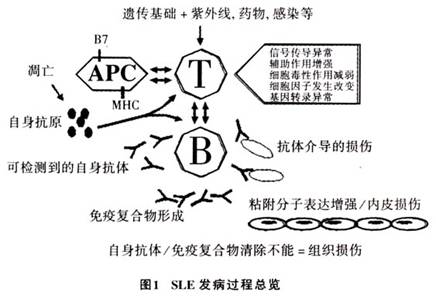
2.SLE�ķ������ƺܸ��ӣ�Ϊ���ֻ���ͻ�����������õĽ��������Ϊ��������ü���Tϸ�������Tϸ���������ټ���Bϸ�������¹������������������������������˵���֯���쳣������ϸ����������������ԭ��һ����ʹTϸ�����ͼ1ΪSLE�������̵ĸ�ͼ��
���߽����Ŵ��Ժͻ����Դٷ����ء��Ա���Լ��ص�Ӱ�졢��������ȱ�ݡ�ϸ�����������쳣�Լ��������������γɺ����߸������쳣�������ڵ�T��Bϸ�����ܸı�Ƚ���������
(1)SLE�Ķ���ģ�ͣ���Ȼ��ϸ�����������ڶ���������SLE�������о����DZ��µķ�Χ�����йش�ҳ��о��Ķ���ģ�͵ı������ϻ������õģ����ҶԱ��º��漸�ڵ�����Ҳ�а�������Щ�������ϵ�Ҫ���ǣ����������ӽ���ģ�͡�������������(NZB)������������(NZW)���ӽ���һ��(F1)�����Ǵ�������������LG/J��AKR/J��C3H/Di����Ŵ�������MRLС��C57BL/6J(B6)��SB/Le������鴿ϵBXSB/MpJ(BXSB)С����3��С�����������ض���С�����ף���Ҫ��������ֳ��
�Ǵ�����(DPLN)���о�������MRL��BXSBС���ڼ����Ǵ��������ĵ�����ͻ�䡣MRL-lpr/lprС��ΪFas���������ܰ���ֳ��ͻ��Ĵ�����С������BXSBС��Я��Y������Yaa����
������SLEһ����������ЩС��������������ds-DNA�������ڵĿ��˿�ԭ�ĸ�ˮƽIgG���������塣��Щ�����������ͨ������С���ԭλ���߸�����������鵼���ס��Ǵ���С��Ҳ��������Դ��xenotropic�����ǵ���gp70������������ԭ�Ŀ��塣��Щ��������Ҳ��С���Ǵ��ķ���������ء�������֮�⣬��ЩС��ģ�ͻ������������ⲡ֢����Щ��֢����������ܰͽ��״�����Ƣ���״���ܰ���ֳ�Բ��䡢
��Ѫ��ƶѪ������������ѪС����١�Ѫ���ס�
Ѫ˨�γ��ؽ��ס�
������С���Ǵ����Ŵ������о�������3��С���н��еġ�ͨ����3��С�������������߲�С������ӽ����п����ҵ�����20���벻ͬ�������߱�����صĻ���λ�㡣��������3����Ҫ���Ǵ��ж����У���������Ҫ��֯�����Ը�����(MHC)�еĻ���������Ǵ��ķ�����λ�ڵ�1��Ⱦɫ���һЩλ�㲻������������3�ֵ�ÿ1��С���У�����������Ҳ���������ǡ�Ȼ������Щ�о���ȷ���������Ի����ͬһ���в������
(2)SLE���Ŵ�ѧ������������SLE��Ҫ��Σ�����ء��йص�֤�����£���SLE���ߵ�����������Լ27%��һ��������Լ15%����һ���������߲�����SLE���ߵ�һ��������1.7%��3%����SLE���������ߵ�һ�������н���0.25%��0.3%��SLE����ͬ��˫��������˫���Ļ���һ���ʸ�10������ͬ��˫��֮�估��ĸ����Ů֮����ٴ��������ơ�
(3)Ŀǰ���о���ʾ��SLE��һ�����ļ�������ȻԼ��5%���ߵķ���Ҳ���ǵ������������ã������Dz��弶����Ӧ�г�ʼ�ɷִ�����ȱ�ݵĻ��ߡ�������SLE��صĺ�ѡ������λ�У�MHC-���ԭ��λ��������¶�ǽ��������(mannose binding lectin��MBL)���ڵ�����������ص�����Ro/SSA��CR1��������Gm��Kmͬ���͡�Tϸ�����塢һЩϸ�����ӡ�Fc���塢���ݿ˵���(HSP)-70����δ��λ���뼲����صĻ����ѡ����
һ��˵�������ݹ��ܿɰ�������SLE���Եĸ���MHC�ͷ�MHC�����Ϊ3�ࣺ
�ٿ��ƶ��ض�������ԭ������������Ӧ��Ļ�����Щ����Ҳ���ܹ�����ٽ���ϻ����������ԭ�ĵ��ס�����͵������ǽ鵼��������T�ܰ�ϸ�����߷�Ӧ��MHC-�������Tϸ���������Ҳ�Ǵ�����ǿ�����ĺ�ѡ�ߡ�Ȼ�����������о������ì��֮�����ڣ�����Ϊֹ����֤�ݱ�����Щ��������ϵ״̬����SLE��������ء�
�ڵ����ܰ�ϸ��������ϸ�����������Ļ���
��Ӱ�����߸����ﴦ���Լ���֢�Լ��������������б���Ļ���������ֲ�����������IgG��������ϸ�����ӻ���ȡ�
(4)HLA��SLE������ԣ�
��MHC-���������MHC��HLA������λ�ڵ�6��Ⱦɫ�峤�۵�һ��λ��߶ȶ�̬�ԵĻ���أ������߷�Ӧ������Ҫ�����á����鵼������T�ܰ�ϸ�����������߷�Ӧ��HLA-���ԭ(A��B��C)�͢��ԭ(DR��DP��DQ)λ���⣬������������л����ɶ��ֲ���ɷֻ���(C4A��C4B��C2��B)��ϸ�����ӻ���[������������(TNF)�����º��ܰͶ���]��ɵġ�
��ȥ��20��30���У�HLA��SLE������������������е��Թ㷺���о���SLE��HLA-���ԭ������ԣ�����HLA-���ԭ����������ƽ�⡣�����༲����صĵ����ʹ��������HLA-DR3��DQ2��HLA-DR2��DQ6��λ����Ȼ������ЩHLA�������е�ÿ1������SLE�����Σ���Խϵͣ�Ϊ2��3����ʾ��MHC���Ŵ���ϵ��ǿ��
�����о�����ͼ���MHC������������������SLE�ٴ�����֮��Ĺ�ϵ��������˵��������ʽ���о���ʾ����������������IJ��������HLA-DQ��λ������к�ǿ������ԡ����磬��SLE��������ۺ�����DQw2.1/Dw6���Ӻ����Խ�Ͼ��뿹SSA�Ϳ�SSB������ء�ͬ����HLA-DQ�µ�λ����(*0602��*0605��*0302��*0303)Ƶ�ʵ������뿹������P������ء����������й�HLA�Ϳ���֬������صı�������Ӣ�����ߵĿ�����֬������HLA-DR4��أ������������ī���综�ߵĿ�����֬������HLA-DR7��ء�ͬ�����б���˵SLE����ԭ���Կ���֬�ۺ������ߵ��Ǵ�������Ϳ�ѪС���ǵ�������HLA-DQ1*06��λ������ء����⣬Carliz�ȵ��о���ʾ��Ӣ������HLA-DRB1*1302��DQB1*0604/5�������뿹��2-GP������ء�HLA�뿹DNA����Sm����U��RNP����֮��������������ӣ��ҽ����һ�¡�
�ڵ��ڵ����Ļ���С��SLEģ�͵��о�֤ʵ��������λ��������������߲���
�Ǵ����ۺ����ķ�������MRLС��lpr����Ĵ���ʹSLE�������������ߡ�lpr����Ϊͻ���fas���������Ϊ�����ܰ�ϸ����ijЩ����ϸ�����������б����ϸ���������塣����fas������ȱʧʱ�������ܰ�ϸ������������ܰͽ��״��
Ƣ����������������С�����ף�ʹ�Ǵ�������١���lpr�����⣬����ͻ��fas����(fas-L)��gld����ҲʹMRLС���SLE�������ӡ������࣬fas��fas-L�������в��϶�����Ȼfas��fas-L����ͻ����������з��֣�����Ȥ���ǣ����Dz�������SLE�����ԣ�����ALPS�������߲����ܰ���ֳ�ۺ�����ء�
�۲���ɷֺ�������Ļ������ڲ���ɷֵ��Ŵ���ȱ����SLE���ر��Ƕ�ͯSLEǿ�������������Ŵ������ء�����ɷ�ȱ�ݶ�SLE���Ե�Ӱ�����в��ġ������صĺͲ���㷺���Ǵ���C1q��C1r��C1s��C4ȱ���йأ�������C2��C3ȱ�������ӻ���Σ���ԡ�C1q��C1r��C1s��C4��C2ȱ���ߵ�SLE�����ʷֱ�Ϊ92%��57%��75%��10%������ȱ����SLE֮������ֹ����ƺ����м�ֵ�ģ���Ϊ������Щ���Ļ��Ƕ�����ӣ���ȻC1r��C1s��12��Ⱦɫ�������ӣ�C2��C4ͬ��MHC-���������λ�С����ֹ����������˵Ļ����д�����������ȱ��Ҳ�����������߸������������������߸������ڸ�����֯�еij��������⣬�Ը�Ⱦ���غ����߸�����������ϰ�Ҳ�ᵼ�������������ӡ�
SLE������֯���ﲹ��CR1����(CD35)��ˮƽ�����йء�����SLE��CR1ȱ���ǻ���Եģ��������Ŵ�������
�ܸ�¶�ǽ�������ػ���¶�ǽ��������(MBL)���ɸ�����Ϊһ�ּ����෴Ӧ���ϳɵ�C��ֲ�������ء��ڽṹ��MBL��C1q���ơ����ɲ���������������IJ��弶����Ӧ����������;����MBLȱ�ݿ�����SLE������Σ���ԡ��о���ʾ��MBL�����54�������ӵ�ͻ��������ӵĶ�̬���������ص�ȱ����ء�
��IgG�����������IgG������3�ࣺFc��R��(CD64)��Fc��R��(CD23)��Fc��R��(CD16)����Щ���Ӿ�ΪIg�������Ա���ڰ�������2��3���ɶ��ϼ�������Ig��ģ�塣���ǵIJ����Ҫ�ڿ�Ĥ���Ͱ�������Fc��R�ڽ鵼���߸��������������Ҫ���á��б���˵�����������SLE���������߸����ﲡ����ȱ�ݡ���Fc��R�Ľ���ڰ�������������Tϸ�������á���ԭ�ݳʺͶ���ϸ�����Ӻϳɵȶ������߹����о�����Ҫ���á�
����������й�Fc��R���Fc��R������̬��֮�������ԡ�Fc��R�����ֱ����Fc��R��a-H 131��Fc��R��a-R 131������λ������������IgG�Ľ����������ͬ��Fc��R��a-H 131������Ωһ����Ч���IgG2�����塣�����Ӹ���������Ч�ش�����IgG2���ɵ����߸������Fc��R��a-R131��IgG2���߸������ϵ�Ч����ϵ͡��б��������������˺�������SLE������Fc��R��a-H 131��λ������١����������R/R131�����͵Ļ��߸����ܷ��������Ͱ���
��Ѫ��ƶѪ�͵Ͳ���Ѫ֢���ڵ��������������Բ��䡣
��Fc��R�������SLE����Ե��о����٣���������б�����1�鲻ͬ����SLE���ߵ��о��з�����Fc��R���µĶ�̬�ԡ�
��ϸ�����ӻ���ϸ�������ڵ�����Һ��ϸ�������к���Ҫ����SLE�����з���TNF-���Ͷ��ְ�ϸ������(IL)�IJ����쳣�����⣬Ҳ��SLE����TNF-����IL-6��IL-1��������(IL-1Ra)��IL-10�����̬�Եı�����
TNF-����SLE�п���Ϊ��Ҫ�ļ����������ӡ���ˮƽTNF-���ƺ��п�SLE���������á�TNF����λ��HLA-�������λ�У�����TNF-����TNF-�º��ܰͶ����Ӧ¡�TNF-�µ�λ������DR2-DQw6֮�����������ƽ�⣬��������TNF-���ĵ�ˮƽ������ء��ɴ���ʾ��TNF-�������Ľ���Ҳ����DR2-DQw6�����
�Ǵ�����������Σ�����йء�֮�����б���˵������TNF����λ��(TNF-2��TNFB
*1��TNFB
*2)�ڲ�ͬ����SLE���ߵ�Ƶ�����ӡ���Ϊ����Щ�����м�������HLA-DR2��������ƽ�⣬����ЩTNF����λ����һ����������SLE���Ժͷ�����˵�����Ƕ�����Σ�����ء�
IL-10���յ�����ϸ����B�ܰ�ϸ����ֳ�ͷֻ������������IL-10��SLE�ķ�չ���ٴ���������һ�����á�IL-10�Ļ�����Լ4Kb���������������2�ֶ��������̬��(IL-10.R��IL-10.G)�����������ڸ��������У�IL-10.G��λ����ķֲ��������IJ�ͬ�����⣬�������ۺ���������ı���Ҳ��ijЩIL-10.G���ǵ�λ������ء���һ���й�SLE�����У�δ����IL-10���������Ӷ�̬�Ժͼ�������֮����ʲô��ϵ��������Щ����-824��-597λ�����ӵĶ�̬������С������������ء�
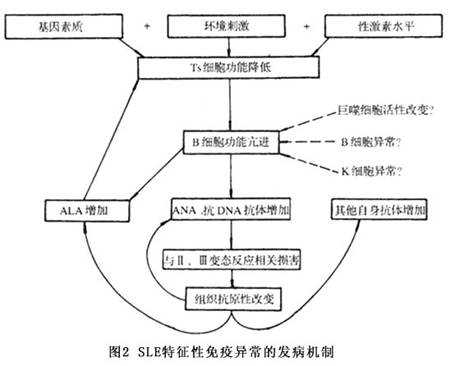
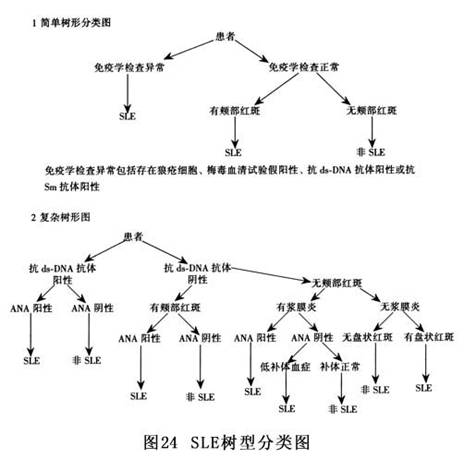
������SLE�������������������Զ��SLE����Ļ������������ٽ��˼�����SLE���о��������������о�δ�۲쵽������SLE��ɢ����SLE���ߵ��ٴ����ֺ�ʵ���Ҽ�������Բ�ͬ����ˣ���������������Ҳ����������ɢ����SLE�����ߴ��������SLE���ߡ��Ӷ��SLE�������������������ҵ���6������λ��(1q22-24��1q41-42��2q37��4p15-16��6p11-22��16q12-13)�����Ƿ��������������ı���������ÿ���о���Ŀ�еļ�������Խ���(17��187)�����ƺ�ֻ��ijЩSLE�л����Ǻ㶨�ġ���֮������ѧ����Ϊ�������쳣���������������(ͼ2)��
3.����
(1)Ƥ��������һ��������ı䣬Լ����4�ܺɳ������Ե���֯ѧ�ı䣬��Ҫ����Ϊ����ϸ������ˮ�ס�Һ�����Լ���Ƥ�ϲ�ˮ�װ��к�ϸ�����������ɼ�������ά���ױ��ԣ������ڿ�����״�Ǵ��������ơ������������ɷ�����ľ��С�壬�����ټ�����ľ��С��Ϊ����������״�����ۺ������LEϸ����������ͬ����Ƥή�������ǻ����Ⱥ�ϸ��������ᡣƤ��֬����֯�����𣬳ʾ������Һ�Ա���ܰ�ϸ�����ɼ�СҶ��ˮ�ͽ�ԭ��ά����ά���ױ��ԡ�
(2)���ࣺ����������֯��
�Ǵ�������Ϊ6�����ͣ���������С�ڵ���ϵĤ�ԣ�ϸ�����������Ѫ��ϵĤ��ëϸѪ�����κθı䣬Ԥ��ѡ��۾���ڶ��ԣ���������С����ֲ��䣬����Ϊ��Ի�����(��)Ӳ������ǰ�߶�����������������ԣ�����������С������ַ�������ͨ��ÿ����С��Ĵ����ۡ�������ϸ������ϸ������������ëϸѪ���ڻ�ëϸѪ���⣬�γ������壬����Ĥ���������ɰ�����С��Ӳ����������Ϊ��С�����Ĥ������Ƥϸ����Ѫ�ܼ���ϸ����ֳ����ϸ������;����Ի�������Ĥ�ԣ�����Ĥ����������Ƥ���������׳�������С��ϸ�����������ԣ�ϸ��������ᣬ������ϸ����������Ӳ���ԡ����ಡ�䲢����������С��Ҳ�ۼ����ʡ���С�ܺ�Ѫ�ܡ������ಡ����ʾΪϸ�������������������顢ϸ���������塢��ϸ����������Ѫ˨����������֢����ʾ��ҩ�����Ʒ�Ӧ�ã���������С��Ӳ������ά�������塢��С��ή����������ά������ʾ��ҩ�����Ʒ�Ӧ�
(3)���ࣺ����Ĥ�ɼ���������״����Ĥ�ף�����Ĥ�½����֯������ά���ױ��Լ��ܰ�ϸ��������άϸ�������ļ����ʡ����ʺͽ�ԭ��ά�����Ե�����ά���ױ��ԣ�����Ĥ�������Ի���������Բ��䣬Լ�������������ۿɼ�����Ĥ�����
(4)Ƣ�ࣺԼ15%�IJ����ɼ��������ԡ����Ƥ������������Ϊ�����Զ�����Χ��ά������ɵġ�
(5)�ܰͽ��ı�Ϊ�������ԣ���Ҫ����Ϊ�����������ɰ��о����Ի������ܰ��ϸ����ֳ�����ٶ�ή�����н�ϸ��������ż���ɼ����������ġ�
(6)��Ĥ�������ʾ������ά�ĵ��׳��ţ�����ϸ����ֳ�����в�ͬ�̶ȵ���֢����λ��Ѫ����Χ����Ҫ�ɵ���ϸ����ɣ�СѪ�ܹ�ǻ������Ƥ���Ͷ�������Ҳ�ɼ������Ե�Ѫ���ף�����ϸ��������СѪ�ܱڡ�
(7)��Ĥ�ͷΣ���Ĥ����֯ѧ�ı�Ϊ��Ĥ������ά���׳��š�����ά��������СѪ���ס��β���Ҫ����Ϊ�����Է�����֯ѧ�ı䣬�ɼ���ˮ������ϸ������Զ�˺�����ϸ֧�������ţ����ݼ���ʰߵ�״ȱ���з�����
�����������⣬���������ɼ��з��ݳ�Ѫ��μ��������ֲ����ɼ��з�����������Լ1/5�IJ������ۼ�С�������������ʻ�����Ѫ���ף�Ѫ�ܲ����Ϊ��֢�ԣ�Ҳ��Ϊ�����ԡ�
(8)���ࣺ�����ֲ��䣬һ�ֱ���Ϊ�����ڼ��Բ����Ը��ı�ġ������Ǵ�������һ�����Ǵ������ף�����֯ѧ�ı���ʾ��СҶ������֯�������ܰ�ϸ������СҶ�ṹ�ƻ�����СҶ�γɣ����������ı�����
��Ӳ����
(9)���⣺����ά�������Ա䡢����ά���ױ��Ժͽ����֯��Ӧ����֢��
(10)���Ӻ�ӫ��������飺
�ٵ��������죺���������ᣬ������������ά������Ĥ������ϸ���ʺͻ���Ĥ��ĵ����������ı䡣���������У��ɼ�����ϸ���ʻ����ͷֽ⣬�ڽ�ԭ��ά�С�СѪ���ڡ���Ƥ���Ƥ���������ɼ������ܵ�����ά���׳������Ʋ�����ǿ�ԭ���帴���
��ӫ��������飺δ���̶��������������ס���C3������Ƥ�����걾���ɼ���IgG��IgA��IgM��C3��Clq���س��š���Щ�ɷֿɵ������ڣ�Ҳ�ɸ��ϴ��ڡ�Լ90%������Ƥ�����걾���ڱ�Ƥ-��Ƥ���紦��������Χ�Ļ���Ĥ����ʾ�������������״��ϸ����״���ţ���Ƥϸ���˺ͽ���ϸ����Ҳ��ӫ����䡣Ŀǰ��֤ʵ�������ֻ��걾����Ĥϴ�ѵ������׳����У����п�����Ĥ�Ϳ��˿�����ԡ�������ɼ�ëϸѪ�ܳʡ���˿Ȧ�������������걾����ֱ������ӫ���鷢�֣���ëϸѪ���Ⱥ�Ѫ�ܼ�������������(��ΪIgG�����ΪIgM����ʱΪIgA)�γɵĴֿ������ţ���Щ���������к��в���ɷ�C3��C4��Clq�ͱ����أ���ʱ��������ά����ԭ��
 �ٴ�����
�ٴ�����
�ٴ����֣�
1.���ڱ��� ���Ծ���������Ů֮��Ϊ1��7��10����������Ϊ2��80�꣬��20��40������������������ж��������������ڿɽ���1���������۵ı��֣�ͬʱ������������(�����ǿ��˿��壬���ANA)���Ե�ʵ���ҷ��֣���ɶԱ���������ṩ�ɿ��������������ٴ����ֱ仯������ʽ��䣬�ɼ�������ͬʱ��Ҳ����̳��ּ�����������ı��֡���������һ����������(��Ⱦ����ɹ�������ܴ̼�)�����������֢״Ϊ���ȡ�ƣ�͡����ؼ��ᡢ�ؽ���(ʹ)���ϳ��������ڱ���ΪƤ�𡢶�Խ�Ĥ�ס����ಡ�䡢������ϵͳ��ѪҺ�쳣��������֢״�ȡ�
2.ϵͳ�Ա���
(1)���ȣ�85%���ϵIJ����ڲ����п��в�ͬ�̶ȷ��ȣ��еĿɳ��ڳ������ȶ�������֢״�����Ե�ʵ���ҷ��֣��������ANA���ԡ����ȶ���ڼ������ߣ����ֲ��˸�����̷���Ⱦ�йأ��������ڳ��ڽ��ܴ�����������ƵIJ��ˣ����������˷���Ϊ�����Ĺ���������
(2)�ؽڼ���֢״���йؽ�ʹ��ռ90%���ϣ���Ϊ�ȷ�֢״���ҳ���Ƥ�𡢷��Ⱥ�����������ͬʱ���������͵�����Ϊ�����ԶԳ��Թؽ�ʹ�����ͣ����ۼ���ָ��Զ��С�ؽڡ�ָ��ؽڡ���ָ�ؽڡ���ؽں�ϥ�ؽڣ�Ҳ���ۼ������ؽڡ������ʪ�ؽ�����ȣ������ؽ��������������죬���������ˣ�������쵽���º��ֿ��ٶȸ������������˺����й�����ʴ�������ƻ����ؽڻ��Ρ�����Ӧ����Ƥ�ʼ��صIJ��ˣ�5%��10%�����ɹ�ͷ���Ź�ͷ������
Լ���������ڲ�����ڿɳ��ּ�ʹ�ͼ������������ϡ���֫�������ԡ�����ͷ����¥��ʱ�ɳ��ּ��������䷢���볤��Ӧ�ô���������йء�Լ10%�����ɷ�����Լ��ס�
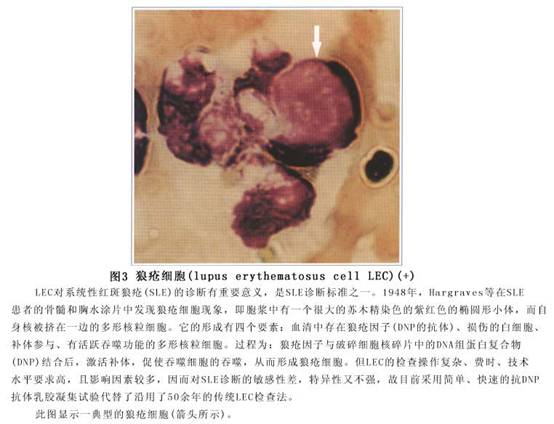
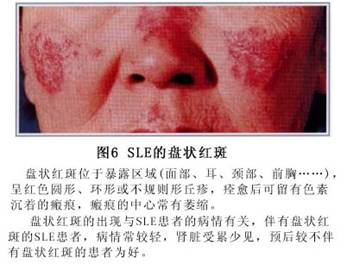
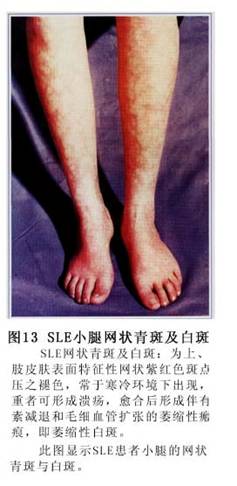
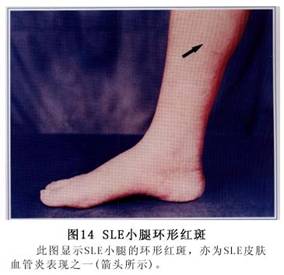
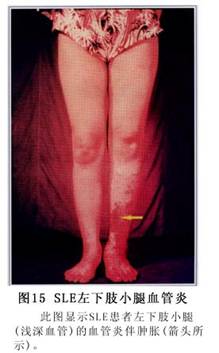
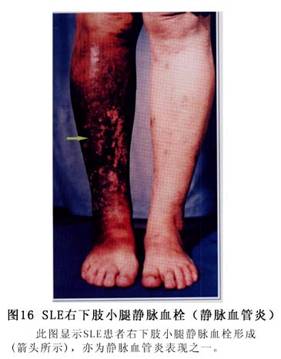
(3)Ƥ����80%�IJ����ɳ���Ƥ������Ƥ��Ϊ��������DZ����������Ա��֡�Ƥ����ֶ��ֶ������к�ߡ����ë�����ˮ�塢Ѫ�塢���塢��ڡ�ëϸѪ�����š�����Ѫ�ߡ���Һ�����á����衢���ҡ�����ή���ȣ���Ϊ����֮һ�ֻ���ͬʱ���Ⱥ�����ȫ���κβ�λ���ɷ���������Ƥ��Ϊ�������沿�ĵ��κ�ߣ��Գ��Էֲ���˫����պͱ�������Ե�����Ϊ��¡��Ľ����Ժ��(ͼ3)������Ϊ
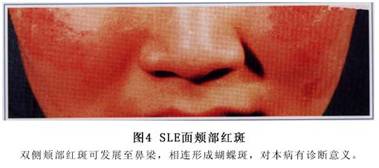
��������ɹ�������Ժ���Ϊ����ɫ����ʱ��߿ɳ���ˮ�����Ƥ����֮����ճ������м��ë�ҽ���˨��ëϸѪ�����š�(ͼ4��5��6)��
Ƥ���ڹ��պ���أ�����1��2��֮���������ˡ�Ƥ�����˺���γ��ۺͷ���ɫ�س��Ż�ɫ����ʧ��ή������ʱƤ����ۼ���˫����ͷƤ�;�����Ƥ����������ڲ�����ڡ�20%��30%�IJ��˶��չ����������Ϊ��ɹ�չ��Ƥ����¶��λ(�沿��ǰ�����)�ɷ���Ƥ�ż������ȫ����
ݡ�����������Ƥ�𣬿ɰ��������л�
��ʹ�С����������ʱ���շ�Ƥ����ϵͳ�Ժ���Ǵ���
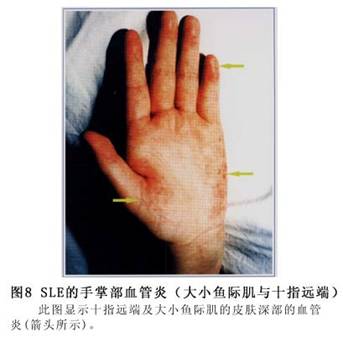
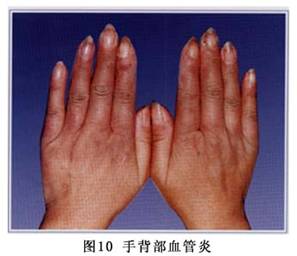
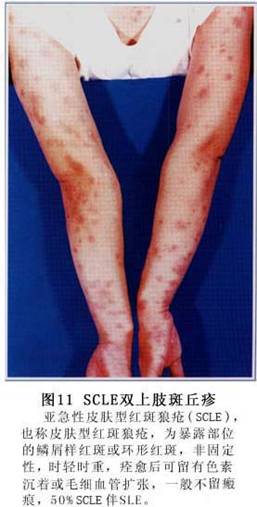
��֫Ƥ��Ҳ�кܴ�������ԣ�����ָ(ֺ)����������Ժ�������ͺ�ëϸѪ�����š���С��ʡ�ָ(ֺ)�����⡢ϥ��������λ(����ѹ)�ɳ��ֳ־��Ժ�ߡ��״�������Ҳ�ɷ�����ߺ�ëϸѪ�����š�Ƥ���ͷƤʱ��������Ƥ���������־���ɥʧ������Ϊ���������ѷ�����֢���˺����²����εĵ�ɫ�����ۡ��ѷ�Ϊ����������Ƥ�𣬶���ڲ����ڣ��ɱ���Ϊ�������ѷ���Ҳ�ɱ���Ϊ�ߵ����ѷ��������͵�Ƥ����ѷ��⣬�п��ڲ��̲�ͬʱ�ڳ���ijЩ�������Գ־��Ի�һ����Ƥ�𣬰������ߺ���ϵ��Ѫ����ѪС��������¡����⣬�пɳ��ִ�����Ƥ�֫��Զ������ͻ��ң�Ҳ�ɷ����沿ˮ�ס�����������
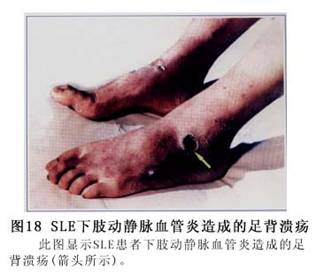
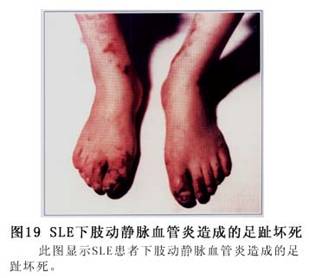
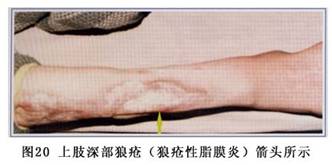
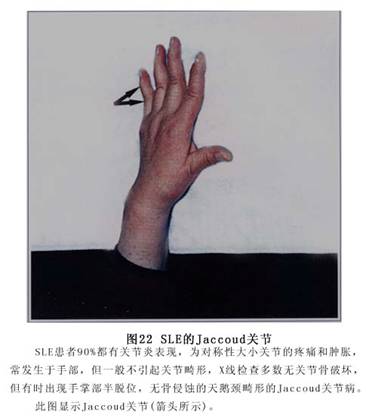
ݡ������ȫ��������ɫ�س��ŵȡ�(��֫Ƥ��仯��ͼ7��8��9��10��11��12��13��14��15��16��17��18��19��20��21��22)��
�еIJ����ڲ����ڿɳ����Ĥ������Ϊ�Ĥ�����ȶ��������ͱ��и���Ҳ�ɷ����������ͺ��Ĥ��Ҳ�ɱ���Ϊ�����ס��Ĥ��Ѫ�����úͳ�Ѫ��Ƭ�����������ɷ���
�ڼ�Ƥ֢��Ƥ�����ʳ��š�������Ҳ�ɷ���Ƥ�����Ƥ��֬Ĥ�ף�����Ϊ������������ʹ��Ƥ�½�ڣ�Ƥ�����ͻ��к�ߣ����Ϻ����а��������γɡ�10%��15%�IJ������ڿ�����ŵ������ӲƤ��������Ϊ�ᡣż���ɳ��ֺ����֫ʹ֢������Ϊ����֫��Ƥ���¶����ߺ���������ʹ��
������������Ƥ��Ϊ���š���״��ߡ�
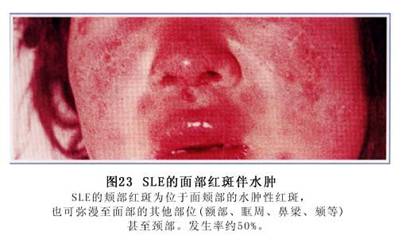
�����Ժ�����ı䡢���ܺ��沿ˮ��(ͼ23)��
(4)ѪҺѧ���������в����ڲ����ж��ɳ���ѪҺѧ�ı䣬������ƶѪΪ���������Ѫ�ܲ��䡢���������ϰ����������ಡ��������йء�Լ10%���˿ɳ�������������
��Ѫ��ƶѪ��������
Ƣ�������±�����Ϊ
Ƣ���ܿ�������Ȼ����
��Ѫ��ƶѪ�ķ����ʽϵͣ�����ʾ����������ֱ��Coomb���������ʸߴ�65%���ϡ����������Զ�������Ѫ�����ߣ����ϸ�����泣����C
3��C
3�ѽ�������Ѫ�����ߣ����ϸ��Ĥ�ȸ���C
3�ָ���IgG����ʱҲ�ɽ�����IgG�����ֿ��������Կ��塣���⣬��������������Ҳ������
��Ѫ��ƶѪ��
��������һ��ѪҺѧ�쳣Ϊ��Ѫ��Ӧ�ķ����ʸߣ��ҷ�Ӧ�̶�Ҳ�����أ������Ա�������ɲ�����ת�Բ������������������ٴ������߱���Դ˸߶Ⱦ��衣���⣬�γɴ�ҪѪ�Ϳ�ԭ�Ŀ���Ҳ�������ߡ������˿ɷ���
�����ϰ���ƶѪ�����Լ������Ʒ�Ӧ���á���ϸ������Ҳ�DZ���������ѪҺѧ���֣�������ϸ�����ܰ�ϸ�������٣������е�Tϸ����Bϸ�����ɼ��١��ܰ�ϸ�������벡���йء������Ը�Ⱦ�ķ�Ӧ�Բ�������ʹ�̷����ظ�Ⱦ����ϸ��Ҳ���������ߡ�������ϸ���������������ڴ��ڿ���ϸ����������°�ϸ���ܽ��ƻ����¡���ϸ�����ٵ�����ԭ���ǹ��������ϰ���ϵѪ���д������ƹ���ϸ���γ��������¡���ϸ���������ķ����м����⣬�����ʵ��쳣������Ϊ���ɹ��ܽ��ͼ�������ϸ���������Ӽ��١�
�ܰ�ϸ�����������ڴ��ڿ��ܰ�ϸ�������йء����ܰ�ϸ�������Ϊ���ࣺһ��Ϊϸ�����Բ���������IgM���壬��4����л��ԣ���һ����ʹ�ܰ�ϸ���������ƻ���
Լ15%������ѪС����٣���Ϊ���ڱ��֣��������ص�Ƥ���Ĥ�������������������ֳ����Ѫ��ż�������ڳ�Ѫ�����ָı����������ڴ��ڿ�ѪС�忹�壬ʹѪС���ƻ���ѭ�������߸�����ʹѪС���˥�����̣�Ҳ�����ѪС����ٵ�ԭ��ѪС�岻�������ļ��٣����һ����ʵ��쳣������ΪѪС�������쳣������ȱ������Ƥ����
Լ10%�������ڴ���ѭ���Ŀ������ʣ�����ߺ������ѪС�����֢�����ɼ���ѪС��������µij�Ѫ������ʹ������Ѫ�»�øʱ���ӳ�����Ѫøԭʱ���ӳ���
(5)���ಡ�䣺��Ϊ�������Ա������г����������ʾ���������������������������ٴ�֢״���Ǵ����ಡ����ҪΪ����
�����ۺ�����
�Ǵ����������˵����пɳ��ֺ�ϸ������ϸ���������͡��������������������Ų����ӳ����������������ڿɳ�����֢����Һ����ʱ���ڸ߱�����ÿ��Ұ��ϸ���Ͱ�ϸ��������5������ʾ����С�����ף�����ж����к�ϸ���Ͱ�ϸ������������5������ʾΪ����������о��������������������ˡ����������ɷ�Ҳ����̳��֣���ʼ���������͡�ϸ�������ͣ��̶����ִֿ������͡���ϸ�����͡���ϸ�����͡�
�Ǵ������ɷ�չΪ
�����ۺ��������ֽ�����ˮ�ף�����֫��ʼ�������ۼ�������֯�������ȡ����߿ɷ���
��ǻ��Һ��
��ˮ��Ѫ���ܵ�����35g/L������/�ױ������ã����ų���ÿ����3g���ϣ�Ѫ���̴�����7.8mmol/L������Ӿʾ��
2�������ߣ��������ڵ���������ʱ���͡��Ǵ�
�����ۺ���������Ĥ����С�����ס���������ֳ����С�����ף�ż���ھ�������ֳ����С�����ס���Ѫѹ��
�Ǵ��������������֣��ɸ������͵����ಡ��������һ�����ָ�Ѫѹ������ζ������IJ����ڶ���ˣ���Ч�ؿ��Ƹ�Ѫѹ���ڿ���SLE�IJ�������Ҫ���á�
����Ҳ�ɷ�����С�����ж����ϵ���С����м��������ף���������С�����ж�����ͨ�����ᡣ����������С�����ж�Ϊ��Ҫ�ٴ���������С��������Ҫ�������߸������������С��������¡���������Ҳ�DZ��������IJ���֢�����ɼ�����ʵ�ʵIJ��䣬���ز��顣���ಡ�����������ܲ�ȫ���DZ���������ԭ��֮һ��
(6)��Ѫ��ϵͳ֢״��ϵ�������������ڽ��ܼ����������¡���������2/3���ϵIJ��ˣ������İ��ס�
�ļ���������Ĥ�ȣ��������İ���Ϊ����������İ��������İ���ά�������ٴ�֢״��֢״���ᣬ������Ϊ������������ʹ������������������ʱ���ż�һ�����İ�Ħ������
�����İ��������İ���Һ�����������İ�����֢״��
2%��8%�����й�״�������䣬ϵ���߸���������ڹ�״��������ֲ�Ѫ���ף����ڽ��ܼ��������������
��֬Ѫ֢�����Ը�Ѫѹ���ڼ������ฺ�ɵ��������𡣳�����Ϊ�Ľ�ʹ���ļ�������˥�ߵȡ�
�ļ������İ����ټ�����ҲΪ��������Ҫ���֣���Ϊȫ����һ���֣������ײ������ഫ��ϵͳ������
�ļ������ٴ�����Ϊ��������
��Ѫ������˥����
����ʧ���ʹ����ϰ�����˥ʱ����ػ�������Ӧ���������ж���Ӧ�ü�����Ӧ���á�
�Ǵ�������Ĥ�׳��ۼ������Ҷ���������������������Ӧ���İ�Ĥ���䣬��Ĥ����Ϊ�����ٴ��ϼ�������Ϊ��ʪ�����ಡ(����겡����������겡�䣬�������ϰ�Ĥ����)��������ƶ�Ĥ�����������˥֢״����ʱ���⣬�����»��������˥֢״���Ӷ����������������Դ���Ѫ����ƹ����߱�����ǰ��ϸ���������Ĥ����IJ���Ȩ���������ס�
���ֲ������ڿ���֫�˾��Ρ�
Ѫ˨�Ծ������ͱ����������ס��������пɷ��������Թ�״���������ȿ�ΪѪ�ܱ����ͣ�Ҳ��ΪѪ�ܱ����͡�������Ѫ���ס������շ���Ѫ֬�����Ը�Ѫѹ�йأ���������ļ����������ʽϸߣ�Ҳ�DZ�������һ����ԭ��
(7)����ϵͳ������50%��70%�IJ��ˣ���Ĥ����ʵ�ʺͷ�Ѫ�ܾ������ۣ���������Ĥ��Ϊ���������Ϊ��������ʹ��������Сʱ�����첻�ȣ���ʱ���в�ͬ�̶ȵ�
��ǻ��Һ����Ϊ����Ҳ��Ϊ˫�࣬�����ۼ��ݸ���Ĥ����ʵ�ʲ����м��ַ������Ըı䣬��ëϸ֧�������š����ݸ��ߵ���ȱ��ȫ�ξ�����С����
�����������Էμ�����ά��������ķι����ϰ�Ϊ������ɢ�����½����λ����½����Ǵ��Է����ۼ��ε�1Ҷ����Ҷ����һ���Է�СƬ״�������������ʧ�������жಿλ�������Ը������������������������ص�֢״Ϊ�����Է����ͽ���ͨ�����ۼ�˫�·�Ұ�����裬�ٴ�����Ϊ�ضȺ������ѡ��������١�ȱ������礣����ַβ�����IJ����ʼ��ߡ��������������μ�����ά��������Ϊ
�����Ժ������ѣ��������ٺ�ȱ�������̳��߿�����
�ζ�����ѹ��
����ëϸѪ��©����������
��Ѫ��������ż�����������صķ��ݳ�Ѫ��
��ˮ������֢״���Ʒγ�Ѫ-�����ۺ��������ֲ��˶��ڶ�����������
(8)����ϵͳ���ɷ����ڰ������ϵIJ���������Ϊ
��ʹ�������Ǵ�Σ��Ϊ���ԣ�������Ϊ����֢���ɰ���
��ˮ���ҳ�����������θ����Ѫ�����DZ���������֢״����Ϊһ���ԡ��������˿ɷ��������Խ᳦�ס�������ʳ���˶��ϰ���
�δ��DZ�����һ�ֳ������������в�ͬ�̶ȵĸι��ܸı䣬���ָı��뼲�����������ʡ�ҩ���ж��йء��Ǵ��Ը������ƺ�ι��ܿɺܿ�ָ�������ҩ��������ͣҩ��ι��ܼ��ָ�������
�δ��߳�����
Ƣ�����������˿ɳ��������״�������Ϊ
�����������ɷ���������ۺ�����
(9)��ϵͳ֢״Լ����50%���ϵIJ��ˣ����ۼ�������ϵͳ���ɳ��ָ�����ʽ�����;���,������֢,���,�������Բ���,�������Χ����ȡ�������ϵͳ֢״��������֢״�����������ڲ����л����ڣ����˳ƴ�Ϊ�Ǵ��Բ���������
����Ǵ���
����Ϊ��������������֮һ��������Ϊ15%����ͯ���߸��ߡ�������ΪSLE��Σ�յļ�֢֮һ���䷢���������Ϊ������������ΪС�����������˶��Է�����ͨ���Կ�������Ʒ�Ӧ���ã���������ȫ����֢״����Ƥ�ʼ������ƿɽ����䷢����ֵ��
��
ͷʹ��Լռ10%���ɱ���Ϊ������
ͷʹ��������
ƫͷʹ�����������ȫ��֢״�緢�ȡ�Ƥ��ȣ��벡���йء�
����Χ���䣺����Ϊ���ָо����˶��ϰ���������֫���Եĸо��˶��ϰ�����֫�����ס��������о����ˣ���ľ��ʹ����ʱΪ��������ʹ���ʹ��������������Ϊ֫�巢���Գ鴤��������ȸо��ϰ�����Χ�����Ϊһ���ԣ������ƺ��没�黺���������ʧ����Щ֢״��������Ϊ�̷���Ѫ���ף�������Ӫ�������������ı仯��
�ݶද֢������Ϊ�赸֢���ɳ�ȫ���Ի�����ԣ���Ϊ��֢״���ɷ���������
���ڸ�ѹ֢������
��Ĥ����ǰ�߱���Ϊ����
ͷʹ��Ż�£����߱���Ϊ
ͷʹ��Ż�¡���Ĥ�̼�����
�߾���ʧ���������ڴ����������������SLE����֢״���������ڲ���Ӿ�ʱ�ų��֡�����ľ���֢״������״̬����һ�ֳ����ľ����ϰ���
�������֢�����֣���������Ѫ���ס������������йء�����������Ԥ��ϲ��������
�մ���
�˸��ϰ���
�����������Դ�������Ϊ���ľ����ϰ��������Ϊ���鵭Į�����ԡ�����
ʧ����ֱ�ӡ�������͡������ٻ������������ʶ���ѡ�����������ȡ����˷�Ϊ���ľ����ϰ�����Ϊ
ʧ�������Ρ��������ǡ��������ɡ�˵�����ϲ������������ӡ���Ц���������������ˡ��������ư���ľ����ϰ�����Ϊ
ʧ�������Ρ��˷ܡ�������ǡ���������֮�ɳ��ֻþ���
����ϰ������֡�������֡��ܾ����Ƶȡ����������ϰ�һ������ڲ����ڡ���Σ�ں����ڣ�������������Բ��䡣
(10)���֢״����������۲�֢״�����۵ı�Ϊ����������Ϊ����Ĥ�а�ɫ��������Ѫ��ˮ�ף�
����ˮ����С������ϸ���߽����������״������ں�ϸ�����塣���ɷ�����Ĥ�ס�dz���Թ�Ĥ�ס�����������Ϊ�������ʹ��
����ŧ����
(11)�ܰͽ�������в�ͬ�̶ȵ��ܰͽ��״���Ҹ�Ѵ��ܰͽ��״�Ϊ���ԣ����Ϊ������ż���ɷ���ȫ���ܰͽ��״������ܰͽ��״����ڷ��š��ݸ���֧���ֲܷ洦�����߿������
��Ҷ�ۺ�����
(12)�Ǵ�Σ��ϵ������һ�ֶ��֡������Ϊ���ȣ�ȫ������˥�ߺ�ƣ��������
ͷʹ��
��ʹ��������ʹ�������и�ϵͳ����������
�ļ���������˥�ߺ�������ϵͳ֢״������Ϊ����������
�������鷢�ֲ���Ⱦ��
��Ѫ֢�ȡ����������ۣ�����˥�߿ɵ���������
 ����
����
���ƣ���Ϊϵͳ�Ժ���Ǵ��ļ����ܹ㣬ÿ���������ֵļ����̶ȼ��ٴ����֡�������������ͬ����˶�ϵͳ�Ժ���Ǵ�������ǿ�����˶��죬ͬʱҪ���ǵ����Ʒ�����Ч��ȣ���ҩӦ���廯��
����Ŀ�ģ�ά�����ٹ��ܣ���ֹ�������ˣ���ʹ���������˼��ᵽ��С�ȣ�ͬʱԤ�����ӻ���ڵķ�����
1.��ҽ����
(1)һ�����ƣ�
�ٽ������ˣ��Բ��˵Ľ���ʮ����Ҫ��ʹ���˶��ú�����ҩ��������õ���Ҫ�ԣ��ò����˽�Ӧ���ݲ���IJ�ͬ���ƶ���ͬ�����Ʒ�����Ӧ���˶��졣
��ȥ������ʱȥ�����ճ��������ܹ��շ������ϵͳ�Ժ���Ǵ��ĸ������أ�������չ���ɹ������Ӵ�������ҩ��(Ⱦ������ɱ���)��ʳ����ٴ̼���ʳ������룬�����������������ݣ����˿ڷ�����ҩ�ȡ�
����Ϣ�Ͷ������ڼ����Ŀ�ʼ���ƽ���Ϣʮ����Ҫ������ҩ���ѳ�ֿ���֢״��Ӧ���ݻ��ߵľ�������ƶ��������˶��ƻ����ɲμ��ʵ����ճ�������ѧϰ�����ݽ�ϣ�������ϡ�
�ܾ�����������ƣ����⾫��̼����������������������أ�����Ҫ�����ʶ�������ij����ԡ������Ժ�����ԣ��ֲ�Ҫ��ǰ;�����˵��ǣ����۲����Ƿ⣬��Ӧ���ڵ�ר��ҽ�������г�����ã���ʱ�õ�ָ�������ܹ�����ѵ�����Ч����
�ݻ������ұ�����
A.�������������䣬�����չ����䣬�Է��������
B.�������˾�����ֹ��Ⱦ����ΪSLE�����ʹ������߹��ܵ��£��ټ��ϳ��ڽ����������Ƽ����ƣ���ֿ�����һ���½������̷���Ⱦ��һ����Ⱦ��Ӧ��ʱȥҽԺ�����ʱ���Ƹ�Ⱦ�����ⲡ�鷴����Ӧ��������ƽʱ�ʵ�ʹ�������������ҩ����ת�����ӡ������صȡ�ͬʱ��Ӧ�������˵�������״̬���������������ܴ̼����������ã�ͨ����-����-�ڷ�������ɼ��ز��飬���������ơ������ٴ��۲죬SLE����һ��������������ز��飬��˲��˵�����ҲӦ����ʹSLE���˱��������������˵�����ҩ������������Ҫ���ر��ڻ�����ά������ʱ����Ҫ��
��ҩ�����ʳ������ǰ����ҩ�����շ������SLE��Ҫ�������������ʹ�á���������ʳƷ��ɼ�������ز��飬ҲӦ��ʳ���ʳ��������������������ʳ��������ز��顣
(2)ҩ�����ƣ�
����Ƥ�ʼ��أ���Ƥ�ʼ���������ϵͳ�Ժ���Ǵ�����Ҫҩ�����������ҩ����Ч���ѻ������Ҫ����(���ġ��ԡ�����)���������¸�Ϊ��ѡ����Ҫ�����ڼ��Ի�ڲ��ˣ��ر��Ǽ��Ա������Ǵ��������Ǵ������ס�����������ϵͳ�Ǵ��Լ��ϲ���������������ƶѪ��ѪС�����������Ƥ�ʼ���Ӧ�õļ����ͷ���������ݻ��ߵľ����������ȷ����ͨ���������÷���
A.����Ʒ���һ��ѡ�ü�������(��ǿ������)1g������Һ���о�����ע��30��60min�ڵ���(������Ϊ������3h�ڵ���Ϊ��)��1��/d������3��5�졣���ڵ�2��������3���ظ�ʹ�á�Ҳ���õ�������ÿ��7.5��15mg���г�����ƣ����������������ʱ��ϳ������ѽ��ٲ��á��Ƴ̽��������������(ǿ����)ÿ��60mg�ڷ����ٴ���Ҫ�����ڼ��Ա�����ϵͳ�Ժ���Ǵ����Ǵ����������������ܶ�Ѫ�����������ߣ��Լ����������Ǵ������Dz��������������Ժ��������Բ��ۺ����Ļ��ߡ�����Ʒ�Ӧע����Ӧ֤������֤�������ü��Ը����õĴ�����
B.������Ʒ����ڷ���һ��ѡ��������ÿ��60��100mg��ÿ��ÿǧ������1��1.5mg���������ȶ�����������Ҫ�����ۼ���Ҫ������ϵͳ��ʱ����������ֳ�����ף��������Ʋ�����ת�������������֯��������������Ч����������Ѫ��ƶѪ��ѪС����������(��50��109/L)�Լ�Ƥ��������Ĥ��θ����֢״���ص�Ѫ���ס��Ǵ��Է������ص������ȡ�
C.�м��������Ʒ�����ѡ����Ч�Ƽ��������ɡ�����������һ�㲻���õ������ɡ��������ɵȳ�Ч�Ƽ�����������������ÿ��20��60mg֮�䣬�ٴ���Ҫ�����ڳ���ʹ�������Ʋ���õ����ÿ��ƺ�ļ�ҩ���Լ���������һ���ڵĻ��ߡ��˽ε����ƶദ�ڼ���Ӧ�ü����ɴ�С�ļ����Σ���ҩʱ��Խ������ҩ�ٶ�ӦԽ�����Ƴ̶��ڰ�����һ�����ϻ���á����ڼ��صĸ�ҩʱ�䣬һ��ÿ����������1�η��ã������ȽϷ����������ڣ��Ӷ����ٶ�������Ƥ�ʵ����ơ����������ԣ�����ڷ������ϴ�ʱ���ɽ�ÿ��������3��(ÿ6��8Сʱ1��)��ҩ��
D.С����ά�ַ�����һ��ѡ��������ÿ��15mg���ڣ�����ÿ��5��7.5mg����С����ά�֣�ͨ������ÿ�쳿��һ�θ�ҩ������ҩ�ķ������ٴ���Ҫ�����ڼ����ȶ��ڵij���ά�����ơ�
���������Ƽ���һ�����뼤�غ��ã�Զ����Ч���ڵ�����Ƥ�ʼ��أ�����ﵽһ�����ۻ�����
A.����������ͨ������Ƥ�ʼ��غ��ã���Ҫ�����Ǵ����������ƣ������������ü�������24���µ���Ч�������ڵ��ü����ߣ�������Ϊÿ��1��2.5mg/kg��ÿ��0.2g����ע�䣬ÿ��2��3�Ρ���������������������Ʒ�(����������0.8��1.2g������Һ���о�����ע��ÿ3��4��1��)���Լ�������֯��ά����һ�����ã�����Ϊ���ȶ������ܺͷ�ֹ������˥�ߵ�һ��ʮ����Ч�ķ�����
B.�����ᵪ��(������)����ϵͳ�Ժ���Ǵ�����Ч��ϻ������������Թ�������ƺ�������Ƥ���ƻ��Լ��ѷ����ϻ�������Ϊ�ᡣ��ˣ���ʱ�뼤�غ��������Ǵ������ף�������Ϊÿ��0.1mg/kg��������400mgʱ��Ӧ������ͣ����ά����Ϊÿ��0.02mg/kg��
C.�������ʣ��������ʶ�ϵͳ�Ժ���Ǵ��϶���Ч�����뼤�غ���ʱ���Ǵ���������һ����Эͬ���ã�������Ϊÿ��1��1.5mg/kg��
D.�����¼���ض�ϵͳ�Ժ���Ǵ��鷢�������ѪС�����������Զ����Ч�������⣬����Ƣ��������һ���ķ��ա���������Ӧ�þ���ע�䳤���¼��Ʒ������Ƣ���ơ�
E.������A��������A��һ������ԵĻ�״���ģ��ܸ��Ű��ذ���(����-2)���ͷź�����T�ܰ�ϸ���Ļ�����ѹ㷺����������ֲ�����������Լ��������ơ�������۸�����һ���������ԣ���Ŀǰ��Ҫ���ھ�����ҩ��������Ч��ϵͳ�Ժ���Ǵ����ߣ���ʼ������ÿ��3��3.5mg/kg����1��2�οڷ����羭4��8����Ч�����ÿ���1��2���£�ÿ������0.5��1mg/kg��������Ϊÿ��5mg/kg��
F.�װ�����(MTX)�����������Ǵ��Բ�ʱ�װ�����5��10mg�ӵ�������5��10mg����ע�䣬��ȡ��������Ч��
G.
��Ϥ������ˮ��Ϊù����֬�����������ʴ�л;���еĴλ����ʺ���������ø�����п�T��Bϸ����ֳ�����ã����������Ե����������ۺ������Լ������ػ�����A������ͣ��ʱ���������ܼ��ˣ�����Ӧ�á�
H.��������(
��������Ϊ��f�����������Ƽ��������û�����Ҫ�����ƶ�������������ø�Ļ��ԣ��Ӷ�Ӱ���ܰ�ϸ������ऺϳɡ�
�ۿ�űҩ��
���0.25g��1��/d�ڷ�����������0.2g��1��2��/d�������߾��п��������ȶ���ø��Ĥ�����ã����Զ�ϵͳ�Ժ���Ǵ������Ƥ��������ؽ�֢״ʮ����Ч��Ҳ��������״�Ǵ�����Ҫҩ��֮һ������Ҫ�ĸ����ð�������Ĥ���䡢�ļ���������ҩ�ڼ�ע����۲�������ĵ�ͼ��
�ܴ����������ע�����ף�ÿ��300��400mg/kg������3��5�죬�����˿�����1�ܣ��������ص�ѪС����٣�����֢�Ǵ��ϲ���Ⱦ�Ļ��ߣ������á�����Ҫ���û���Ϊ������Fc����鵼�ĵ�����״��Ƥϵͳ���ƻ����ã��������Ϳ������ã�����Th1/Th2�Լ�һЩϸ��������IL-1�ķ��ڡ������ã�ż�з��ȡ�Ƥ���Ѫѹ��һ��������������
��ϸ�����ӣ�ϸ���������弰�������͵���¡���������Ŀǰ��������Σ���Ϊϵͳ�Ժ���Ǵ��������ṩ���µľ��顣
��
Ѫ���û�����������������Σ��������ϵͳ�Ժ���Ǵ����������Ǵ����������Ǵ����ס�Ѹ�ٷ�չ�������ۺ������߶�����ߣ���Լ����������Ƽ�������Ч������Ӧ�ý����߿ɿ��ǡ�������ÿ���û�
Ѫ��40ml/kg��ÿ��3�Σ���2��6�ܣ�ͬʱ��Ӧ���������Ƽ���
��Ѫ��ϸ����ֲ����Ѫ��ϸ����ֲ�������ؽ���ʹ���������ϵͳ����ʶ��������ԭ����ͨ����ѡ��������������ܣ�ʹ��������������Կ��ƣ�ĿǰҲ�������ٴ�����Ρ�
���Լ��أ�������(������)��һ�������ۼ��أ��������Ǵ���ѪС�������Ч����Ҫ�������������ס��¾�������
���֢���ƣ����������۷�����Ѫѹʱ��Ӧ�����ʵ���ѹ������̷��������ܲ�ȫ���µ�ˮ����������ҡ�������֢ʱӦ��ѪҺ���Ʒ�����������硢������Լ�����ʧ��ʱ����ȫ�����ƵĻ����ϣ�����Ӧ�ý⾷����Ӫ����ҩ�� ���ͱ���(³����)��B��ά������ȡ�����������˥��ʱ���ɸ���������
��ػ���Ѫ������ҩ����Эͬ�������ƿ�����˥���м̷���Ⱦʱ��Ӧ��ʱѡ�ÿ�ԭ����С�Ŀ����ؽ��п��ơ��������������߲����ű���״���ס����������ص�ʱ����Ӧ�����ص��ļ��������ʵ����ơ�
��ֲ����ƣ�
A.Ƥ�������ͬ��״�Ǵ���
B.�۲����䣺���ü��ػ��������Ƽ�����ȫ�������⣬�п���
�ɵ�����ҩˮ�ֲ���λ��ü����������Ĥ����ע�䣬��ʱ����֢״��
2.��ҽ����
(1)��֤���Σ�
���ȶ���ʢ��
��֢���沿�����ɡ���֫�����ʺ죬���ȳ������ˣ����꣬��࣬�ڿʣ�����������辪�ʣ����dz�Ѫ����Ѫ��Ƥ���ϰߣ�С��Ƴ࣬����ؽᣬ���ʺ�筣�̦�ƣ�����ϸ��������
�η������Ƚⶾ����Ѫ���ߡ�
��ҩ��Ϭ�ǵػ�������ζ�������Ӽ���
����30g������20g����Ƥ20g��������30g������20g���ѹ�Ӣ20g���ض�20g��Ұ�ջ�10g����ʯ��30g���ϲ�20g������20g���������30g��ˮţ�Ƿ�5g(��)��
�Ӽ�����������ߣ���
����ţ������
��ѩ�������ʿ����ߣ�������ۡ����١�����ĸ���dz�Ѫ������Ѫ�ߣ��Ӳ��Ҷ�������ܡ����߷۵ȡ�
���������ȣ�
��֢�����Ȳ��˻����ҹ�䳱�ȣ����еȶȷ��ȣ�ʱ��ʱ�ͣ��沿����֫����ʱ��ʱ�֣���ϥ��ʹ��ͷ�ζ��������ķ��ȣ��ڸ�����������ѷ����¾����ڡ����ٻգ�С��ƣ����ɣ������̦��̦���ƣ���ϸ����
�η����������ȣ��ⶾа��
��ҩ������������ζ��
����15g�����15g(�ȼ�)������30g��֪ĸ12g����Ƥ20g��Ů����15g��������20g������20g����20g�������15g����ޱ15g���ع�Ƥ15g���������30g���̶���30g��
�Ӽ�����ϥ��ʹ��ɽ���⡢��ţϥ���������ؽ���ʹ����ܴ��ʯ�������������ķ��ȼӻưء�ĵ�ã�ҹ�²����ӳ����ʡ�ҹ���١��ϻ�Ƥ������ĸ�ȡ�
���������飺
��֢��ȫ���������ɴ�������ί�ң��ļ£����̣������أ�������ʹ���ѷ����ڸɣ�����������䣬�Ժ������������ᣬ�൭�����ʺ죬��̦���ף���ϸ����ϸ����
�������������
�����10g(����ҷ�)����20g����ζ��10g������30g����Ƥ12g������12g������20g������15g��������20g�������15g��ɽ����12g��ɽҩ15g������12g��
�Ӽ���������䡢�Ժ������ߣ���ĵ�á���С����Ƹ���������ʹ���ѷ��ߣ��Ӵ�ţϥ����˿�ӡ��������Ļ����̡���ϸ���ߣ��ɺ����˸ʲ�����
�ܷ�ʪ�ȱԣ�
��֢����֫���⡢�ؽ���������ʹ���ʣ������ؽں�����ʹ��ʹ���ɴ������첻�����ɰ��з��ȣ�Ƥ���ʺ�����ϼ��ӳ��֣����̦��������������
�η�����绯ʪ�����Ⱥ�Ӫ��
��ҩ�����������������ɢ�ϰ���֦���Ӽ���
����20g��ɣ����30g������12g���ư�12g������30g����ţϥ20g����ʯ��30g��֪ĸ12g����֦10g����ܴ12g��������30g����ܺ12g��
�Ӽ����ؽ����������ߣ��ӳ�ǰ�ݡ����ߡ���к�������ӽ����������̡��ѹ�Ӣ��
��������Ƥ���ʺ��ߣ������ء���Ƥ��ˮţ�Ƿۣ�Ƥ���ϰ�����֫�������ߣ���
��������Ѫ�١������ȡ�
�ݸ���Ѫ����
��֢���沿�������ߡ�ɫ����в����ʹ���ʹ������Ʀ�������ͣ��ɲ��в����֢�飬���㣬��鷺��������ͷ��ʧ�ߣ�Ů���¾����������վ��������ϰ����������㣬����ϸ���ϸ��ɬ��
�η�����ν�������Ѫ������
��ҩ��������ɢ�Ӽ���
���24g����10g������12g���㸽10g������12g������10g������15g����Ƥ12g���Ӻ���15g��
����20g������12g�����߷�3g(���)���ʲ�10g��ݭ��6g��
�Ӽ���в��֢���ߣ��Ӵ��zhe���裻�����ߣ�����¡���֦��������ݡ���
��������ͷ����ߣ��Ӱ��ġ���Ƥ�����ӣ�������ֻ�����������������ߣ�����ݡ���é���������ܵȡ�
��а�����ģ�
��֢���ļ����磬�Ժ�������������ʹ���ķ���ƣ��ʧ�߶��Σ��沿�����ɡ���֫����ʺ�죬��鷴�����ȣ�����ϣ�֫����������ʹ�������һ����չ���վò����ɵ����κ�֫�䣬��ɫ�ף����ٲ�������ϸ����ϸɬ�������������죬��֫���䣬��������
�η������İ���Ѫ�ܶ���
��ҩ���������ĵ���
�������Ӽ���
̫�Ӳ�30g����20g�����Ŷ�20g����ζ��10g��
����20g������12g������15g������20g��������30g��̴��10g������12g���˸ʲ�10g����ܺ12g��������6g��
�Ӽ������ơ���ʹ�ߣ��ӹ�¨��ޯ��ӷ�
�����պ�����
��Ч������������ϡ����ٲ��������Ƥ�������ӣ����п����ߣ���ɣ��Ƥ���˰ٲ������ݣ��������ѣ���֫���䣬�����죬�������ߣ��˼���
�����
�ײ������壬��������10��15g���ϣ�Ҳ���òθ���ĵ����
�θ�ע��Һ�������ơ�
��Ƣ�����飺
��֢�����漰��֫���ף�������֫Ϊ������ϥ�������κ�֫�䣬��ɫή�ƣ���ƣ�뵡������ʳ�٣����٣������߿ɳ�����������գ��ر����٣�����ƽ�ԣ�����̵������ģ��ļ����٣��������ۡ��ʵ�����̦���ף�����ϸ����
�η���������Ƣ��������ˮ��
�츽��12g�����6g������20g������30g������12g����ػ�20g��ɽ����12g��ɽҩ15g������20g����к20g����ǰ��20g(��)����ţϥ20g��
�Ӽ���ȫ�����������ߣ������ߡ���С�������Z�������ȴ��ߣ�������ơ������ӡ����ӣ����͡���������ߣ��Ӵ�Ƥ������ͷ�������������١�����ߣ�������Ƣ�����ĩ(����1��2g���)�����ִ�ҽѧ�Ķ�֢�����ȴ�ʩ���м��ȡ�
(2)�ۺ����ƣ�
�������Ʒ���
ȡѨ���������ء�������̨��̫�塢���ء��ٻᡢ���������Ϊ��������ؽ���ʹ��Ϲȡ����ӡ�����Ȫ��Ƥ������ᡢ��Ϫ���������������������м����ķ��������ж���
�뷨���������ء�������̨��1.0mmֱ�����룬����4h������Ѫ����Ѩǿ�̼������롣
3.����
(1)�������⣺�ؽ����ؽ���ʹ�����ȡ�ƣ�Ͳ��ʣ�Ƥ�����ֹ����С���ߡ���ǻ���ǻ���Ĥ�����ϰߡ�ˮ�塢ݡ�����Լ�Ѫ������ˮ�ף�Լ��20%���˻������ŵ����������˥�ˣ��ķι��ܼ��ˣ������쳣��Ӫ���������������ˡ���Ѫ��
(2)����Ŀ�꣺����ؽ���ʹ���ʡ��������£������������ʸС�Ԥ��Ƥ�������Ԥ�������ܶ�ά���ķι��ܡ����Ӱ�ȫ��ʩ��Ԥ�����ⷢ����ά���ʵ���Ӫ������ߵֿ������ṩ����֧�֡�
(3)������ʩ��
�ٱ����ؽڣ�����ؽڵ���ʹ���ʣ��������˶���Ϣ����Ӧ����̶�������ƽʱӦά����ȷ�����ƣ�ÿ��Ӧ���ʵ��Ļ���Ա��������Ĺؽڻ�ȡ�������ע��ؽڲ�λ�ı�ů��
�ڽ������£����ᷢ�ȵIJ��ʸУ����ڷ��Ȳ��ˣ�Ӧ���Ų����Դ���Ϣ���������£��Դٽ�ɢ�ȡ��������û��ˮ������������ˮ����ȡ�����Բ��䷢��֮ˮ��ɥʧ���������ʹ�ã��Խ������¡�
�۱���Ƥ���������������䣺A.����Ƥ����࣬���B.��������ֱ�����䣬���ճ���Ӧ��ɡ�����ھֲ���¶��λ��Ӧʹ�������˹�����ʹ�����˹����ã����پֲ��ܴ̼���C.ÿ����Ƥ�����Ա㷢���µIJ��D.�ֲ�ʹ��Ƥ����̴����࣬��������֢��Ӧ��E.ָ������ƽʱ����������ҩ�ھֲ����ϴ��ˮҲ���ɹ��ȣ�ϴ��ʱ����ʹ�÷������Լ��ٶ�Ƥ���Ĵ̼���
�ܼ���ֲ�֢״��
A.�沿���ֺ���ߣ�Ӧ��������ˮϴ��������Ƥ����࣬����30�����ҵ���ˮ��ë����ɴ��ʪ���ڻ�����3��/d��ÿ��30���ӣ��ɴٽ��ֲ�ѪҺѭ������������м���䡣�沿���ü��Է�������ױƷ���࣬��ֹ�Ծֲ�Ƥ���̼������������
B.Ƥ���Ⱦ�ߣ�Ӧ����ϸ���������ٴ����֣������崴��Ȼ��ֲ�����Ӫ����������ҩ��ʵ�Ӧ�ÿ����أ��ٽ����ף�������Ƥ�����ϡ�
C.�ؽں졢�ס��ȡ�ʹ�����ߣ����û����������ϴ�����ǵĽ���Һʪ������������ֹʹ��
D.�������ѷ��ߣ�ÿ������ˮϴͷ2�Σ���ϴ�߰�ĦͷƤ��
E.���п�ǻ�Ĥ�����߿�ѡ������
����ɢ������˪����룬���ֲ��˿�ǻ���������и�Ⱦ�ߣ�����1��5000
�����Һ���ڣ��ֲ�Ϳ��
����ɢ��
����ɢ�ȣ����������Ⱦ�ߣ�������ù���ظ�����Ϳ��
F.�ݳ�Ѫ���dz�Ѫ������é���������裬��ǻ��Ѫ�϶࣬��
��������������ѹ��ֹѪ���ڷ���ź֭��������֭�뱭��1������Ѫ������Ҫ�۲�Ѫѹ�����ʣ�Ҫ����Ѫ����������Ѫ��
G.ע��������࣬ÿ����1��5000
���������Һ��ԡ���û���15g��������15g����ˮ��ϴ���Է������Ĥ���á�
��Ԥ�������ܶ�
A.�����������ܼ���ʱ��Ӧ���ٻ����������Ѫ��͵������ڼ䣬Ӧ�Դ���Ϣ��
B.ÿ��ע�����������صı仯�������������١��������ӻ���ʱ��Ӧ����ˮ�ֺ��η���ȡ���������������ҽʦ��
C.��������й��л�����������Ϊ���ͣ���ʹѪ�����ص�����������ʱ��Ӧ��ȡ�͵�����ʳ��
D.ÿ�����Ѫѹ��ע��۲��Ƿ����ķθ��ɹ���(Һ���������)��Ѫѹ��֢״��
E.���ѳ���������˥�ߣ�����Ҫ���Ŷ���ѪҺ����Ĥ�����ƣ����ų����ڵĴ�л�����ˮ�֡�
��ά���ķι��ܣ�Ԥ���ķι���˥�ߡ�
A.��ʱע����������ĩ��ѭ���ı仯������Ѫѹ���ߡ����ɲ��롢�İ�Ħ�����Լ�֫��ˮ�ס���������Σ�ӦѸ�ٸ���ҽʦ���Ա�ʩ��ҽ�ƴ�����
B.ע��������Ƿ�ͨ���������ֺ������٣��������˰���λ��������
�������롣�����Ĥ��ˮ���أ����ܻ�ʩ����Ĥ���̷�Һ�����Լ��ٶԷ����ѹ�ȡ������������ܡ�������ʹ�������������࣬������ͷ֧�л����Լ�����ʹ��
�߰��Ű�ȫ��ʩ��Ԥ�����ⷢ����
A.�۲첡���Ƿ�����Ϊ�ı䡢��ʶ���ҡ��þ���������������ȶ����鴤��������������������Ӧ�ʵ��������ˣ��Է����������䴲�»�ҧ����ͷ�����ⷢ����
B.ע��Ƥ���Ƿ����ϰߡ����ߵļ���ƽʱӦ������ײ����˶�������Ѫ��ֹ��
��Ӧ�ü������Ƶ�ע�����
A.��Ƥ�ʼ��ؼ���Ӧ���У�����ͻȻͣҩ����뻼����ҽ����ҩ�����������Լ���
B.����Ԥ����Ⱦ�������ǻ�Ĥ��������������ϵ�Լ�Ƥ���ĸ�Ⱦ��ע��۲����±仯����ǿ��ǻ���������ڴ�����ǻ�ڵĸ��ֲ��䡣��ÿ����л�������࣬��ֹ��������ϵ���и�Ⱦ��
C.�ʵ�����Ƽ���ά����D�����ι������ɡ�
D.ע����Ѫ�Ǻ����ǣ��Է�ֹҩ�������������������Ӧ��ʱע��������֢ͪ��
E.�۲�����ɫ��θ����֢״�����ڼ����DZѪ���Ա����ڷ�����������Ѫ������Ҫʱ����
������������������θ�Ĥ��
F.��Ƥ�ʼ���������������֢״�����з������ҩ������ǿ��ȫ��ʩ��ר�˿�������ֹ�����˺���
G.��������س������ǰ��Ӧ���߽��������ڼ�Ӧע������������ע��������Һ���٣��۲����ɱ仯����ֹ��Һ�ٶȹ��죬��������˥�ߡ�
�Ჹ��Ӫ����������δ����������˥��֢״��Ӧ����������ȡ������ʳ������ÿ����ȡ�ʵ���ˮ�֡���������ѳ���������˥��֢״����Ӧ���Ƶ����ʡ�����ʳ���Լ��Ρ�ˮ�ֵ���ȡ���������л�������Ӽ�ˮ����������������IJ��ʡ�
����辫�������ϵ�֧�֣�����SLE��ͬʱ�ַ�ȫ�������٣��ڷ������˳��в��ظУ��Ҳ��̺ܳ������ܲ�����꣬��ˣ�������Աƽʱ����Ӧ�����ػ��⣬ҲӦ���辫���ϵĹ������������������ڲ�����ǰ����ʹ�á��Ǵ���һ�ʣ��������Ӳ��˵Ŀ־�Ͳ�����
4.��Ժָ��
(1)Ԥ����Ⱦ���ر��Dz������Ϻ�������Ⱦ��Ӧע��Ԥ����Ŀǰ��֤ʵ������������в������ͣ��������𤲡�����ر���C������SLE�ķ����йء�
(2)Ԥ�����䣺���߾�ס�ķ���Ӧע�����º�ʪ�ȣ�һ���¶��˱�����25��28�棬�����������Ȼ�磬��ʹ�ÿյ�������ҲҪ������28�����ϣ�ʪ����50%���ϡ�������ϴ�¡�ϴ�ˡ�ϴ�־�Ҫ����ˮ����Ҫʱ����Ƥ�������ס�ƽʱ���ܽ�ʳ�䶳ʳƷ���䶳���ϡ�����Ҫ��ů����������������ǿ���·������ס�ñ�ӡ����ӣ���Ҫ�����������ڣ���ò�Ҫ�����������ŵ����Ļ��߸�Ӧ�ص㱣�����Դٽ��ֲ�ѪҺѭ����
(3)������գ�Ҫ�����չ���ɹ�����������䣬�����Ҫ��������ñ����̫��ɡ�����������죬ҲҪ����ˮ��ǿ�������������ɵij��¡����㡣�����г����ʻ����ʱҪ�����ס�Ů�Ի��߾�����Ҫʹ�û�ױƷ����ʹҪ�ã�ֻ��ʹ�÷������ߵĻ�ױƷ���ھ�ס�����һ���������Ҫ����ֱ�����⣬����ð�Ҷ��������ס��Ҫ���������Ӿ����ɽ����ˮԡ�ͻ�ѩ�ȽӴ�ֱ��������˶���
(4)����ҩ�Ŀǰ��֪��20����ҩ��������Ǵ����ۺ�������Ӧ���ػ����ʹ�������(�±����)��
��³��������ù����
�ǰ�ҩ������Ӣ(����Ӣ��)�ȣ����ⷢ��SLE��
(5)����ͷ���ǰ���ָ�������߽����й�SLE���йؼ���֪ʶ�������ʹ�����Ҳ���������������������һ�������Ӧ��ҽԺ��⣬���������ڵı���ָ����ʹ����˳���ȹ������ж�֢�ѹأ�����ȷ�������Լ���Ԥ��������Ӧ��֯���ͥ��Ա����Э�̣����������������IJ��˼���������˵����ʹ֮�õ��ɷ�ͳ����������֧�֡�ҽԺ�ڡ���Ҫ��֧֯������ϵͳ����Ҫʱ�ɽ����ݽ��������¼���м�ͥ���ʡ�ͬʱҪָ��������������ʹ�ø��ֱ��з�����
(6)������Ӧ�������Ԥ�����֣���ҽ����ҩ���������ͣҩ����ҩ�����������������ȷ�Ĺ��ܶ������Իָ��ؽڹ��ܣ����ڸ��顣



 ���в�ѧ
���в�ѧ
 ����
����
 ��������
��������
 �ٴ�����
�ٴ�����






 ����֢
����֢
 ʵ���Ҽ��
ʵ���Ҽ��

 �����������
�����������
 ���
���

 �������
�������
 ����
����
 Ԥ��
Ԥ��
 Ԥ��
Ԥ��